
对超过100,000例结直肠癌病例和154,000例健康对照的分析发表在《自然遗传学》(NatureGenetics)上,发现了数百种可能作为新的治疗和预防目标
对超过100,000例结直肠癌病例和154,000例健康对照的分析发表在《自然遗传学》(NatureGenetics)上,发现了数百种可能作为新的治疗和预防目标的信号。
该论文称,这项研究的规模是之前全基因组关联研究的两倍。此次合作包括隶属于欧洲、北美和亚洲数百家研究机构的研究人员,其中包括克利夫兰诊所基因组医学研究所副主席斯蒂芬妮·施密特(StephanieSchmit)博士、公共卫生硕士。这种规模的全基因组关联研究有助于研究人员识别与结直肠癌相关的基因以及受这些基因影响的生物学途径。
“这是理解结直肠癌遗传易感性的复杂性的重大进步,”施密特博士说,她在大约十年前的博士培训期间首次开始从事这项工作的一部分。“这些数据揭示了一些可能具有预防和治疗该疾病潜力的途径,并为探索结肠外的机制(例如免疫系统)提供了持续的加强。”
Schmit博士是本研究的第一作者,代表美国国立卫生研究院资助的结直肠跨学科研究(CORECT)U19CA148107。
结直肠癌是从结肠内壁的生长物(称为息肉)发展而来的。这种疾病每年影响全世界超过190万人。尽管通过家族遗传的一些罕见突变与结直肠癌的高风险相关,但大多数导致结直肠癌的遗传变异在人群中很常见,并且每种变异本身都会增加很小的风险。结合环境和生活方式因素以及癌症筛查行为,遗传学是解决这种复杂疾病的重要难题之一。
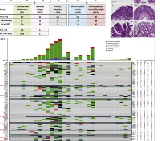
研究人员比较了结直肠癌患者和非结直肠癌患者的基因组数据,以确定与该疾病的遗传关联。该研究通过分析基因组、转录组和甲基组数据确定了250个独立的风险关联,其中50个以前未被发现。分析还发现了155个高置信度效应基因,它们编码影响生物活性的分子。
在识别出这些基因后,研究人员可以检查哪些与风险相关的基因会导致结肠粘膜以外的其他组织发生变化,结肠内衬的组织是癌性息肉生长的地方。结果显示超过三分之一的效应基因最有可能在结肠粘膜外起作用。
该研究还发现,结直肠癌的风险源于分子水平上正常结直肠功能的变化:稳态、增殖、细胞粘附、迁移、免疫和微生物相互作用。
研究结果表明,已识别的基因可能影响多个系统,包括心血管、神经和免疫功能。该论文称,肠道微生物群也是未来研究的一个潜在兴趣领域。
Schmit博士说,新的分析和持续的合作是可以转化为临床实践的研究工作的“跳板”。
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们