
布法罗大学药学院的研究人员最近在分子与细胞蛋白质组学上发表了文章,描述了他们在鉴定参与癌细胞对吉西他滨 (Gem) 耐药性的关键代谢调
布法罗大学药学院的研究人员最近在分子与细胞蛋白质组学上发表了文章,描述了他们在鉴定参与癌细胞对吉西他滨 (Gem) 耐药性的关键代谢调节因子方面的工作,吉西他滨 (Gem) 是胰腺双腺癌的标准护理化疗(PDAC),最致命的胰腺癌类型。
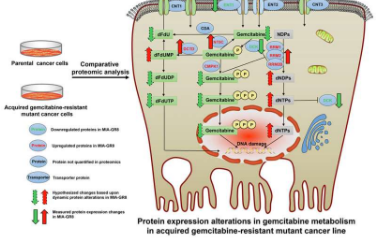
UB 杰出教授 Robert M. Straubinger 博士和药学系教授 Jun Qu 博士领导了这项研究,其中包括纽约州立大学的 William J. Jusko 博士特聘教授和他的几位实验室成员。
吉西他滨耐药性 (GemR) 可在化疗期间在临床上发展,导致患者预后不良。了解 Gem 耐药性的分子机制一直具有挑战性。
Straubinger 和 Qu 合作应用尖端的综合定量蛋白质组学分析方法来识别 PDAC 中 Gem 抗性的关键代谢调节因子。他们的团队系统地检查了 PDAC 癌细胞,并确定了耐药性的几个治疗弱点,这些弱点可以用于改善经历 Gem 耐药性的 PDAC 患者的治疗结果。
胰腺癌对目前的治疗或对某些癌症效果良好的新型免疫疗法反应不佳。Gem 是 PDAC 患者的主要药物,但仅提供适度的生存益处。在临床上,Gem 耐药性的发展可能会很快并影响其疗效。
第一作者 Qingxiang (Nick) Lin,博士——作为 Straubinger 研究所罗斯威尔公园综合癌症中心癌症应激生物学项目的研究生,他完成了大部分工作,现在是麻省总医院/哈佛医学院的博士后学者-开发了多种获得高度 Gem 抗性的癌细胞系。
然后,该团队采用详细的蛋白质组学分析来检验他们的假设,即在开发的细胞系中 Gem 敏感性的非常大的损失将识别出多个蛋白质功能网络,这些网络在 PDAC 细胞中合作以产生高度耐药状态。
总的来说,这项工作对 Gem 耐药性有了更全面的了解,并为设计有效的治疗方法以克服 PDAC 患者的 Gem 耐药性奠定了合理的基础。
关键发现表明,在高 GemR 细胞中观察到的多种蛋白质水平变化的总体结果是,多种药物反应网络的改变协同工作,以降低 Gem 及其活性代谢物的细胞内浓度。
该团队注意到细胞 Gem 运输和代谢途径中蛋白质表达的显着升高,这将防止 PDAC 细胞经历致命的 Gem 诱导的压力和损伤。该团队得出结论,调节这些药物代谢途径的方法可以在治疗上克服 PDAC 患者的 Gem 耐药性,并且一直致力于确定可能协调 PDAC 细胞总体耐药反应的潜在“主调节因子”。
“这项研究利用尖端的全球定量蛋白质组学分析系统地剖析胰腺癌获得性和内在耐药性的分子机制,并提供系统级的见解,可以转化为药物代谢的治疗调节以克服化学耐药性经常在临床上发展,并改善胰腺癌患者的治疗,”林说。
“了解癌细胞的多种途径中存在适应性,使我们能够专注于能够对抗耐药性的新药。一个明显的重点是确定可能驱动耐药性的‘主调节器’,因为我们在高度耐药性中观察到的变化耐药 PDAC 细胞似乎朝着一个总体目标协调。寻找能够重新编程耐药细胞的药物将是利用这些发现并逆转临床耐药性的关键,”Straubinger 说。
该团队继续致力于开发有前途的药物组合策略,可以逆转PDAC 患者肿瘤的耐药性。最终的希望是这些方法可以迅速进入临床研究,使胰腺癌患者与这种高度侵袭性且通常致命的癌症作斗争。
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们