
首先,秦伟伟等人。通过进行多层转录组学搜索,确定肝细胞 NLRP3 是肝脏 IR 的关键诱导剂,并进一步证实其在 NAFLD 患者和小鼠模型(
首先,秦伟伟等人。通过进行多层转录组学搜索,确定肝细胞 NLRP3 是肝脏 IR 的关键诱导剂,并进一步证实其在 NAFLD 患者和小鼠模型(高脂饮食(HFD)、瘦素受体缺陷( db / db)小鼠),以及棕榈酸(PA)诱导的肝细胞。随后,体内研究表明,HFD 诱导的小鼠中肝细胞特异性 NLRP3 功能的丧失或获得分别改善或加剧了肝脏 IR 和脂肪变性。
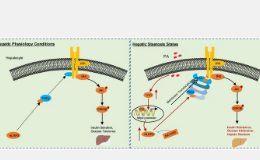
从机制上讲,NLRP3 直接结合并促进蛋白激酶 C ε (PKCε) 激活,从而损害胰岛素信号传导并增加肝脏脂肪变性,而抑制 PKCε 则削弱了 HFD 诱导的 NLRP3 缺陷小鼠中所见的有益效果。此外,我们进行筛选发现转录因子阴阳1(YY1)正向控制NLRP3的表达。这些发现促使科学家们探索治疗潜力,腺相关病毒血清型 8 (AAV8) 介导的肝脏中 NLRP3 敲低可减轻db/db小鼠的肝脏 IR 和脂肪变性,而药物抑制 NLRP3 可显着减轻饮食引起的代谢紊乱。
该团队确定了 NLRP3 驱动肝脏 IR 和脂肪变性的新机制。这一发现揭示了之前意想不到的通过NLRP3 诱导从 YY1 到 PKCε 的代谢疾病调节轴,并将 YY1-NLRP3-PKCε 轴确立为 NAFLD 的潜在治疗靶点。
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们