
来自Organoid 小组(前 Clevers 小组,Hubrecht 研究所)的研究人员与来自 Princess Máxima 儿科肿瘤学中心的研究人员一起建立
来自Organoid 小组(前 Clevers 小组,Hubrecht 研究所)的研究人员与来自 Princess Máxima 儿科肿瘤学中心的研究人员一起建立了脂肪肝疾病的新型人体类器官模型。他们使用这些模型来阐明药物反应,并建立了一个 CRISPR 筛选平台来识别新的疾病介质和潜在的治疗靶点。这些模型将有助于测试和开发治疗脂肪肝的新药,并有助于更好地了解疾病生物学。该研究结果将于 2023 年 2 月 23日发表在Nature Biotechnology上 。
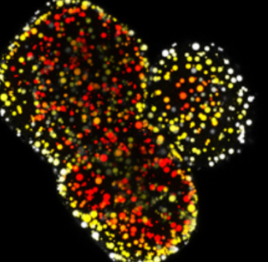
脂肪肝
肝脏脂肪堆积是一种全球范围内越来越普遍的疾病,全球超过四分之一的人口受到影响。患有脂肪肝会导致炎症、肝功能受损,并最终导致疤痕组织形成。不同的原因会导致脂肪肝的发展,饮食和生活方式是最常见的因素。此外,遗传学可以发挥重要作用。例如,遗传性脂质紊乱使患者更容易患上脂肪肝,而一些突变会增加患这种疾病的风险。
无治疗
令人担忧的是,目前还没有可以阻止或逆转脂肪肝的治疗方法。随着疾病的进展,不可逆肝损伤的风险和肝移植的需要大大增加。此外,患有脂肪肝的人患肝癌的风险更高。由于缺乏模型系统,确定解决该疾病的方法非常具有挑战性。小鼠的新陈代谢差异很大,因此不能用作人类疾病的代表性模型系统。此外,目前以人为基础的 体外 模型有几个缺点。这些模型的遗传改造很困难,目前不可能快速生成大量细胞。
脂肪肝类器官
现在,研究人员转向类器官建立三种模型,捕捉脂肪肝发展的不同触发因素。首先,他们用混合脂肪酸“喂养”类器官以模仿西方饮食,并见证了脂肪肝类器官的快速发展。作为第二个模型,该团队使用一种名为 prime editing 的新 CRISPR 工具将脂肪肝疾病的最高风险突变引入了他们的类器官系统。具有这种突变的类器官比没有它的类器官表现出更严重的脂肪堆积。最后,研究人员还使用 CRISPR-Cas9 对遗传性脂质紊乱进行了建模,以研究这些紊乱如何影响脂肪肝的发展。由于糖衍生脂肪的积累,这些突变的类器官自发地发展出严重的脂肪肝。
发现新的药物靶点
该团队随后在新开发的类器官模型上筛选了大量治疗脂肪肝的候选药物。有趣的是,研究人员观察到不同的脂肪肝类器官模型对药物的反应非常相似。通过这样做,他们确定了对所有模型都有效的药物子集。有趣的是,这些有效药物通过一种共同机制发挥作用,即阻止糖类生成脂质。重要的是,该团队还观察到,具有脂肪肝最高风险突变的类器官对所有药物的反应方式与没有突变的类器官不同。这表明类器官可以用作个性化医疗的工具。
CRISPR平台
研究人员继续使用他们的类器官模型建立了一个基因筛选平台,以识别在脂肪肝疾病中起作用的新基因。研究人员将他们的类器官转化为一个名为 FatTracer 的 CRISPR 筛选平台。他们使用这个平台来研究特定基因丢失对脂肪肝表型的影响,可以在 20 天内实时可视化。在对 35 名候选者进行筛选后,发现了 FADS2 基因(脂肪酸去饱和酶 2)在脂肪肝疾病中的一个新的关键作用。FADS2 的破坏使类器官脂肪含量更高。该团队想知道相反的情况,即拥有更多的 FADS2,是否会对疾病有益。事实上,当过表达 FADS2 时,类器官曾经显示的脂肪肝严重减少,
未来发展方向
这些新型脂肪肝类器官模型为未来的许多方向铺平了道路。例如,研究人员希望更好地了解与脂肪肝发展相关的遗传风险,以及研究影响疾病进展的因素。最终目标是使用这些模型来定义(个性化)药物疗法,以治愈肝脏脂肪超载。
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们