
一个国际研究小组首次重建了26亿年前著名的CRISPR-Cas系统的祖先,并研究了它们随时间的演变。结果表明,恢复活力的系统不仅有效,而且比当
一个国际研究小组首次重建了26亿年前著名的CRISPR-Cas系统的祖先,并研究了它们随时间的演变。结果表明,恢复活力的系统不仅有效,而且比当前版本更通用,并且可能具有革命性的应用。NatureMicrobiology发表了这项研究的结果,在研究团队看来,这“为基因编辑开辟了新途径”。
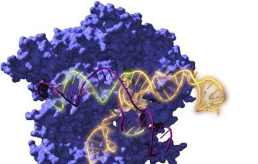
该项目由CICnanoGUNE的Ikerbasque研究教授RáulPérez-Jiménez领导,涉及来自西班牙国家研究委员会、阿利坎特大学、罕见病网络生物医学研究中心(CIBERER)、RamónyCajal医院-IRYCIS和其他机构的团队国家和国际机构。
首字母缩略词CRISPR是指存在于细菌和古细菌(原核生物)DNA中的重复序列。在重复序列中,这些微生物含有来自感染其祖先的病毒的遗传物质片段;这使他们能够识别重复感染并通过使用与这些重复相关的Cas蛋白切割入侵者的DNA来保护自己。它是一种抗病毒防御机制(CRISPR-Cas系统)。这种识别DNA序列的能力是它们有用的基础,它们就像分子剪刀一样。如今,CRISPR-Cas技术可以将遗传物质片段剪切并粘贴到任何细胞中,从而可用于编辑DNA。
当前的研究工作重点是在全球最遥远的地方寻找具有独特特性的新版本CRISPR-Cas系统。为此,探索了生活在极端环境中的不同物种的系统,或者应用分子设计技术来修改它们。寻找新系统的一种完全不同的方法是在过去寻找它们,这实际上是这项研究的基础。
nanoGUNE的纳米生物技术小组由RaúlPérez-Jiménez领导,多年来一直在研究蛋白质从生命起源到今天的进化。对已灭绝生物的蛋白质和基因进行祖先重建,以了解它们具有什么品质以及它们是否可以用于生物技术应用。这是一次通过生物计算技术进行的时光倒流之旅。在这项刚刚发表在《自然微生物学》杂志上的工作中,首次重建了CRISPR-Cas系统从26亿年前的祖先到现在的进化史。
研究团队对祖先的CRISPR序列进行了计算重建,合成了它们,并研究并确认了它们的功能。“令人惊讶的是,我们可以重振数十亿年前一定存在的Cas蛋白,并发现它们当时已经具备作为基因编辑工具的能力;我们现在已经通过成功编辑人类细胞中的基因来证实这一点,”解释说LluísMontoliu,CSIC国家生物技术中心(CNB-CSIC)和CIBERER的研究员,以及在培养的人类细胞中对这些祖先Cas蛋白进行功能验证的团队负责人。
该研究的另一个有趣发现是,随着时间的推移,CRISPR-Cas系统逐渐变得更加复杂,这是该系统具有适应性的标志;它一直在逐渐适应新的病毒威胁,这些威胁在整个进化过程中一直笼罩着细菌。
“这项研究标志着关于CRISPR-Cas系统起源和进化的知识取得了非凡的进步。关于病毒的选择压力如何在数十亿年的时间里微调基本的、最初不是非常有选择性的机器;这一直发生直到产生了一种复杂的防御机制;它是一种能够非常精确地区分自己的DNA的机制,它必须保留它,而不需要的入侵者的遗传物质,它必须摧毁,”阿利坎特大学研究员FrancisMojica说,他发现了CRISPR-Cas技术。在应用方面,“这项工作代表了一种开发CRISPR工具的原始方法,以生成新工具并改进现有生物体中现有工具的工具,”Mojica补充道。
“目前的系统非常复杂,适合在细菌内发挥作用。当系统在这种环境之外使用时,例如在人体细胞中,它会被免疫系统排斥,并且还有某些分子限制限制了它的使用。奇怪的是足够了,在祖先系统中,其中一些限制消失了,这使这些系统对新应用具有更大的通用性,”Pérez-Jiménez说。
HRYC-IRYCIS-CIBERER遗传学服务负责人MiguelAngelMoreno说:“祖先核酸酶可能具有的独创性,只要它不特别识别基因组的某些区域,就可以将它们变成更通用的工具来纠正直到现在还无法编辑或没有非常有效地纠正的突变。”他的团队开发了MosaicFinder工具,该工具通过大规模测序和生物信息学分析,能够表征这些祖先Cas在培养的人类细胞中进行的基因组编辑的效果。
nanoGUNE项目的研究员YleniaJabalera说:“这项科学成就可以使基因编辑工具具有不同于现有工具的特性,并且更加灵活;这为DNA操作和疾病治疗开辟了新途径,例如如肌萎缩侧索硬化、癌症和糖尿病,甚至是疾病的诊断工具。”
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们